Actualité bibliographique de septembre
Revue d'études par Irène Gallais Sérézal, François Aubin, et Julie Charles
Reprogrammer le métabolisme des acides gras poly-insaturés via FADS2 dans les keratinocytes module l’inflammation psoriasiforme, par un mécanisme PPAR-a dépendant.
Cai J, Zhou X, Zhuang Y, Cui L, Ma R, Chen Y, Yang N, Chen Q, Wang Y, Zhu P, Yao L, Yu Q, She X, Zhou X, Huang Y, Yu Z, Zhang X, Lu J, Shi Y, Guo C. Reprogramming of Fatty Acid Metabolism via PPAR α-Orchestrated FADS2 in Keratinocytes Modulates Skin Inflammation in Psoriasis. Adv Sci (Weinh). 2025 Aug 29:e17049. doi: 10.1002/advs.202417049.
https://pubmed.ncbi.nlm.nih.gov/40878384/
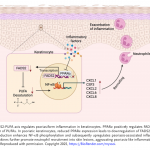
Dans cet article, les auteurs reviennent sur la dérégulation des acides gras poly-insaturés, qui ont précédemment été impliqués dans la pathogénèse du psoriasis. La désaturase d’acides gras FADS2 est abaissée dans le psoriasis humain et les modèles murins de psoriasis. L’absence de FADS2 dans les keratinocytes humains aggravait l’inflammation déclenchée par l’exposition à des cytokines. De façon similaire, une suppression spécifique de Fads2 dans les keratinocytes aggrave l’inflammation psoriasiforme murine (imiquimod) et sa surexpression était protectrice, via une diminution de la synthèse d’acide docosahexaenoique (DHA). Ces observations étaient dépendantes de l’expression de PPAR-alpha. L’activation pharmacologique de PPAR-alpha diminuait ainsi l’inflammation psoriasiforme via la surexpression de Fads2. Au total, cet article identifie un axe d’action potentielle PPAR-alpha/FADS2 pour moduler l’inflammation keratinocytaire (localement?) dans le psoriasis.
Voir Figure 1.
Le PPBP des macrophages du tissue adipeux exacerbe l’athérosclérose liée au psoriasis en induisant une dysfunction mitochondriale dans les cellules endothéliales aortiques.
Zhu L, Du L, Wu J, Ding D, Wang J, Wang R, Liu Z, Kuzmina N, Wang H, Yang Y, Ståhle M, Landén NX, Li S, Li D. Adipose tissue macrophage-derived PPBP exacerbates psoriasis-associated atherosclerosis by inducing mitochondrial dysfunction in aortic endothelial cells. J Invest Dermatol. 2025 Aug 29:S0022-202X(25)02396-6. doi: 10.1016/j.jid.2025.05.041.
https://pubmed.ncbi.nlm.nih.gov/40886963/
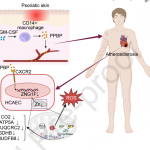
La PPBP (pro-platelet basic protein) macrophagique est élevée dans le tissu adipeux des patients psoriasiques. En utilisant des souris, une analyse de l’aorte dans sa totalité a été réalisée, et montre que les souris sans PPBP ont non seulement moins d’inflammation psoriasiforme (imiquimod) mais aussi moins de plaques athéromateuses. L’administration d’imiquimod (locale) ou de PPBP (injecté) augmentaient au contraire l’athérome aortique. Le mécanisme semble être l’induction d’une dysfunction mitochondriale (régulateur de zinc ZNG1F).
Voir Figure 2.
Anti-IL23 oral: Essai FRONTIER-2
Ferris LK, Bagel J, Huang YH, Pink AE, Tyring SK, Kokolakis G, DeLozier AM, Li S, Shen YK, Iaconangelo C, Ota T, Bissonnette R. FRONTIER-2: A phase 2b, long-term extension, dose-ranging study of oral JNJ-77242113 for the treatment of moderate-to-severe plaque psoriasis. J Am Acad Dermatol. 2025 Mar;92(3):495-502. doi: 10.1016/j.jaad.2024.10.076.
https://pubmed.ncbi.nlm.nih.gov/39549848/
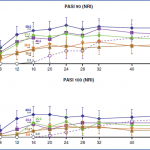
Il s’agit de l’extension à 52 semaines de l’essai randomisé initial FRONTIER-1 comparant le placebo à un peptide oral ciblant l’IL-23. Les résultats obtenus à 16 semaines à la dose de 2 x 100 mg/j se poursuivent à 52 semaines avec un PASI 90 observés chez 64 % des patients et un PASI 10 chez 40% des patients. Les effets secondaires restent inchangés avec principalement des infections naso-sinusiennes.
Voir Figure 3.